胃癌her2阳性晚期,赫赛汀耐药的患者请留意
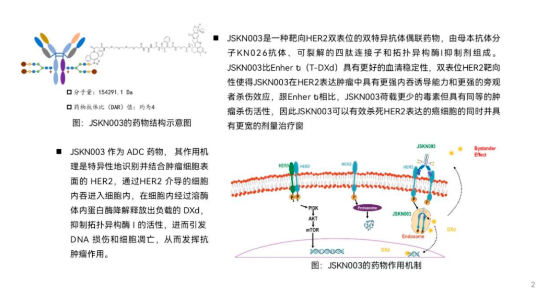
药物介绍:JSKN003 是一种靶向 HER2 双表位的双特异抗体偶联药物,由母本抗体分子 KN026 抗体、可裂解的四肽连接子和拓扑异构酶 I 抑制剂 DXd 组成。JSKN003 比 Enhertu(T-DXd)具有更好的血清稳定性,双表位 HER2靶向性使得 JSKN003在 HER2表达肿瘤中具有更强内吞诱导能力和更强的旁观者杀伤效应,跟 Enhertu 相比,JSKN003 荷载更少的毒素但具有同等的肿瘤杀伤活性,因此JSKN003 可以有效杀死 HER2 表达的癌细胞的同时并具有更宽的剂量治疗窗。效果跟DS8201相当,毒性比较低,没有8201常见的血液毒性和间质性肺炎。
试验药物:JSKN003
简单入排:
1. 受试者经组织学或细胞学确诊为局部晚期或转移性HER2 阳性的胃癌患者,≥18 岁
2. 首次给药前 7 天内实验室检测或 28 天内心脏超声检查满足以下标准:
骨髓功能:
中性粒细胞绝对计数 ≥1.5 × 109/L,血红蛋白 ≥9.0 g/dL,血小板计数 ≥100 x 109/L;
血常规检查前 14 天内未接受输血或生物反应调节剂(如促粒细胞、红细胞
生长因子等)治疗;
肾功能:
血清肌酐≤1.5 × ULN,或血清肌酐清除率≥60 mL/min(根据 Cockcroft-Gault 公式计算);
肝功能:
总胆红素≤1.5 × ULN;
转氨酶(ALT/AST)≤3 × ULN(肝转移受试者≤5 × ULN);
消化道肿瘤受试者需白蛋白≥28g/L;
凝血功能:
INR 或 PT≤1.5 × ULN;• APTT ≤1.5 × ULN(接受抗凝治疗受试者应采用稳定剂量的抗凝药物);
心脏功能:首次给药前 28 天内经心脏超声确认左室射血分数(LVEF)≥50% ;
3. 同意提供足够的肿瘤石蜡切片或新鲜组织标本进行检测。
4. 研究者根据RECIST v1.1评估存在至少1处可测量的病灶。
5. ECOG体能状态评分为 0 或 1。
试验中心:杭州
患者受益:
⭐可抢先获得国际前沿新药使用机会,对晚期肿瘤患者来说可能是新的生机;
⭐入组后相关的检查、治疗、用药均为免费,大大减轻家庭经济负担!
⭐大型三甲医院一线专家团队为你的治疗保驾护航!
注:做了基因检测的病友可以拿出报告看看,一旦存在突变,可以扫描下方二维码添加专员看看是否有机会接受国内新药治疗,看不懂的病友也可以添加专员解读报告。也可加入“阳光易家亲–肿瘤患友群”或者相应的靶点患友群,与上万位肿瘤患友/家属分享经验,互通有无。




 浙公网安备 33010602004553号
浙公网安备 33010602004553号


